Reizdarm und Darmmikrobiom: Was die Forschung wirklich weiß
Aktuelle Forschung zeigt: Bei IBS fehlen Schutz-Bakterien, während Pathobionten überwiegen. Drei Mechanismen erklären die Symptome.
Reizdarm und Darmmikrobiom: Was die Forschung wirklich weiß
Reizdarm-Syndrom (Irritable Bowel Syndrome, IBS) ist eine der häufigsten funktionellen Darmerkrankungen weltweit. Schätzungsweise 10 bis 15 Prozent der Bevölkerung sind betroffen. Die Diagnose ist klinisch, die Behandlung oft unbefriedigend und die zugrundeliegenden Mechanismen komplex.
Eine aktuelle Übersichtsarbeit in Frontiers in Immunology fasst den Forschungsstand zur Rolle des Darmmikrobioms bei IBS zusammen und leuchtet die Verbindungen zwischen Dysbiose, Darmbarriere, Immunsystem und Gehirn-Darm-Achse aus.
Das Mikrobiom von IBS-Patienten: Was fehlt, was zu viel ist
IBS-Patienten zeigen konsistent ein verändertes Darmmikrobiom. Die Studienlage ist zwar heterogen, aber einige Muster sind wiederholbar repliziert worden.
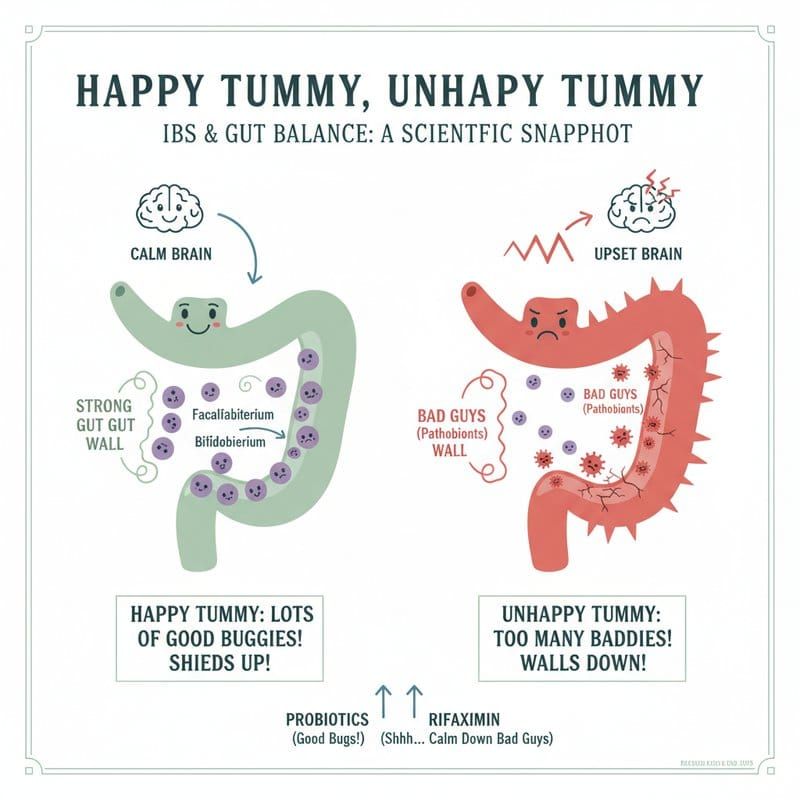
Reduziert sind vor allem Bifidobacterium und Faecalibacterium, beides Bakterien, die kurzkettige Fettsäuren produzieren und entzündungshemmend wirken. Faecalibacterium prausnitzii, bekannt als einer der wichtigsten Darmbeschützer, ist bei IBS-Patienten häufig depletiert, besonders bei dem Subtyp mit vorwiegend Durchfall (IBS-D).
Erhöht hingegen sind Enterobacteriaceae, Lactobacillus und Bacteroides. Auffällig sind auch Pathobionten wie Desulfovibrio (produziert Schwefelwasserstoff, der die Darmschleimhaut schädigt), Fusobacterium und in einigen Studien bestimmte E.-coli-Stämme.
Die drei Hauptwege: Barriere, Immunsystem, Gehirn-Darm-Achse
Das Mikrobiom beeinflusst IBS über mehrere parallele Pfade.
Der erste Pfad verläuft über die Darmbarriere. Butyrat-produzierende Bakterien wie Faecalibacterium und Bifidobacterium stärken die Tight Junctions, jene Verbindungsproteine, die die Darmepithelzellen zusammenhalten. Bei IBS sind diese Verbindungen oft gelockert. Das Ergebnis: erhöhte Darmpermeabilität, Durchtritt von Lipopolysacchariden in die Blutbahn, niedriggradige systemische Entzündung.
Der zweite Pfad verläuft über das Immunsystem. Veränderte Gallensäurenzusammensetzung, verursacht durch dysbiose-bedingte Umwandlung von primären in sekundäre Gallensäuren, aktiviert Mastzellen in der Darmschleimhaut und löst Entzündungsmediatoren frei. Mastzellen bei IBS-Patienten sind näher an Nervenfasern lokalisiert und hypersensitiv.
Der dritte Pfad führt über die Gehirn-Darm-Achse. Das Mikrobiom produziert Neurotransmitter und Neurotransmitter-Vorläufer: Serotonin (90% davon werden im Darm produziert), GABA, Dopamin. Veränderte Mikrobiomsignaturen verschieben diese Neurotransmitter-Balance und beeinflussen Schmerzschwelle, Darmmotilität und emotionalen Zustand.
Post-infektiöses IBS: Ein klarer Auslöser
Eine besonders gut belegte IBS-Untergruppe ist das post-infektiöse IBS (PI-IBS). Nach einer akuten Gastroenteritis entwickeln rund 10 Prozent der Betroffenen ein dauerhaftes Reizdarm-Syndrom. Das Risiko ist 3,5 bis 4,2-fach erhöht im Vergleich zu nicht-exponierten Personen.
Die Mechanismen: Die Infektion hinterlässt Dysbiose, erhöhte Darmpermeabilität, residuale mukosale Inflammation und in manchen Fällen Anti-Vinculin-Antikörper, Autoantikörper gegen ein Darmprotein, das Darmmotilität reguliert.
Therapieoptionen: Probiotika, Rifaximin, Low-FODMAP
Die Übersichtsarbeit bewertet auch die Evidenz für mikrobiombasierte Therapien.
Probiotika zeigen in einigen Studien Wirksamkeit bei Bauchschmerzen und Blähungen, aber die Effektgröße ist moderat und stark stammspezifisch. Die 2025 Seoul Consensus on IBS Management bewertet Probiotika als schwache Empfehlung mit sehr niedrigem Evidenzniveau.
Rifaximin, ein nicht-absorbierbares Antibiotikum, ist für IBS-D in den USA zugelassen und wirksam bei globaler Symptomreduktion, Stuhlkonsistenz und Bauchschmerzen. Sein Wirkmechanismus ist teilweise mikrobiomvermittelt: Es moduliert Bakterienpopulationen ohne systemische Absorption.
Die Low-FODMAP-Diät verändert das Mikrobiom: Sie reduziert die Abundanz fermentierbarer Substrate und damit gasgene Bakterien. Studien zeigen, dass Basismikrobiomprofile das Ansprechen auf Low-FODMAP vorhersagen können.
Was noch fehlt
Trotz des Fortschritts: Die IBS-Forschung hat das Mikrobiom noch nicht als therapeutischen Endpunkt etabliert. Es fehlen ausreichend große RCTs, die gezielt Mikrobiomveränderungen als primäre Endpunkte messen. Die Heterogenität der IBS-Subtypen erschwert generalisierende Aussagen.
Die einfache Erklärung
Reizdarm ist keine Einbildung und keine reine Stresskrankheit. Bei Menschen mit Reizdarm fehlen wichtige Schutzbakterien im Darm, und dafür haben sich schädlichere Bakterien vermehrt.
Das hat Folgen: Die Darmwand wird durchlässiger, das Immunsystem ist ständig leicht aktiviert, und die Kommunikation zwischen Darm und Gehirn läuft nicht mehr rund. Das erklärt, warum viele Reizdarm-Betroffene auch unter Ängsten, Stimmungsschwankungen und Schlafproblemen leiden.
Gute Nachrichten: Bestimmte Probiotika und Diäten können helfen, das Gleichgewicht wiederherzustellen. Aber was genau für wen hilft, ist noch nicht vollständig verstanden.
Quellen
Autor et al. (2025). Gut microbiota dysbiosis in irritable bowel syndrome: mechanisms and therapeutic implications. Frontiers in Immunology. Frontiers in Immunology, 2025
